時間:2025-07-24 作者:X-MOL【轉(zhuǎn)載】
注:文末有研究團(tuán)隊簡介及本文作者科研思路分析
靶向蛋白質(zhì)降解旨在消除失調(diào)的蛋白質(zhì)��,已成為征服具有挑戰(zhàn)性的治療靶點的一種有前途的策略��。蛋白水解靶向嵌合體(PROTAC)是一種異雙功能分子�,它利用泛素-蛋白酶體系統(tǒng)選擇性降解靶蛋白����。由于其能夠在不引起耐藥性的情況下降解“不可成藥”的蛋白質(zhì),PROTAC 在創(chuàng)新藥物開發(fā)中顯示出巨大的潛力��,尤其是在癌癥治療方面��。然而,常規(guī)結(jié)構(gòu)的 PROTAC 存在一些局限性����,例如生物利用度和藥代動力學(xué)有限、腫瘤靶向能力有限��、非特異性毒性和鉤效應(yīng)�。因此,對常規(guī) PROTAC 進(jìn)行結(jié)構(gòu)創(chuàng)新以使其滿足治療需求對于釋放 PROTAC 作為治療工具的全部潛力至關(guān)重要����。近日,新加坡國立大學(xué)陳小元����、鄒建華/天津大學(xué)王生/清華大學(xué)喻國燦合作總結(jié)了非常規(guī)結(jié)構(gòu)PROTACs的設(shè)計,用于應(yīng)對上述挑戰(zhàn)和提高癌癥治療療效�。
蛋白質(zhì)作為細(xì)胞基本功能的主要執(zhí)行者,在維持機(jī)體正常功能方面起著關(guān)鍵作用�。包括癌癥在內(nèi)的各種疾病都與蛋白質(zhì)穩(wěn)態(tài)異常相關(guān)。因此��,對失調(diào)蛋白進(jìn)行干預(yù)是一種具有創(chuàng)新性和突破性的治療方法�����。蛋白水解靶向嵌合體(PROTAC)由于具有治療效果更完整和持續(xù)、可針對“不可用藥”蛋白的靶向降解�����、降低耐藥等優(yōu)勢�����,在癌癥治療中得到了廣泛的研究��。但常規(guī)結(jié)構(gòu)PROTAC面臨生物利用度和藥代動力學(xué)有限�、腫瘤靶向能力有限��、非特異性毒性和鉤效應(yīng)等局限性����。
為了應(yīng)對上述挑戰(zhàn),充分發(fā)揮PROTAC治療潛力����,研究者們提出了許多策略來開發(fā)“非常規(guī)PROTAC”。根據(jù)不同的結(jié)構(gòu)��,本文總結(jié)了癌癥治療中的四種非常規(guī)PROTACs����,包括非常規(guī)靶蛋白結(jié)合配體的PROTACs����、非常規(guī)連接體的PROTACs���、pro-PROTACs和自組裝的PROTACs�����。本文還討論了非常規(guī)PROTACs在臨床治療中的挑戰(zhàn)和未來發(fā)展方向�,旨在鼓勵進(jìn)一步探索優(yōu)化PROTACs的功能模塊�,為更高效、更有選擇性的靶向蛋白質(zhì)降解策略提供方向���,拓展其在未來臨床腫瘤治療中的應(yīng)用����。
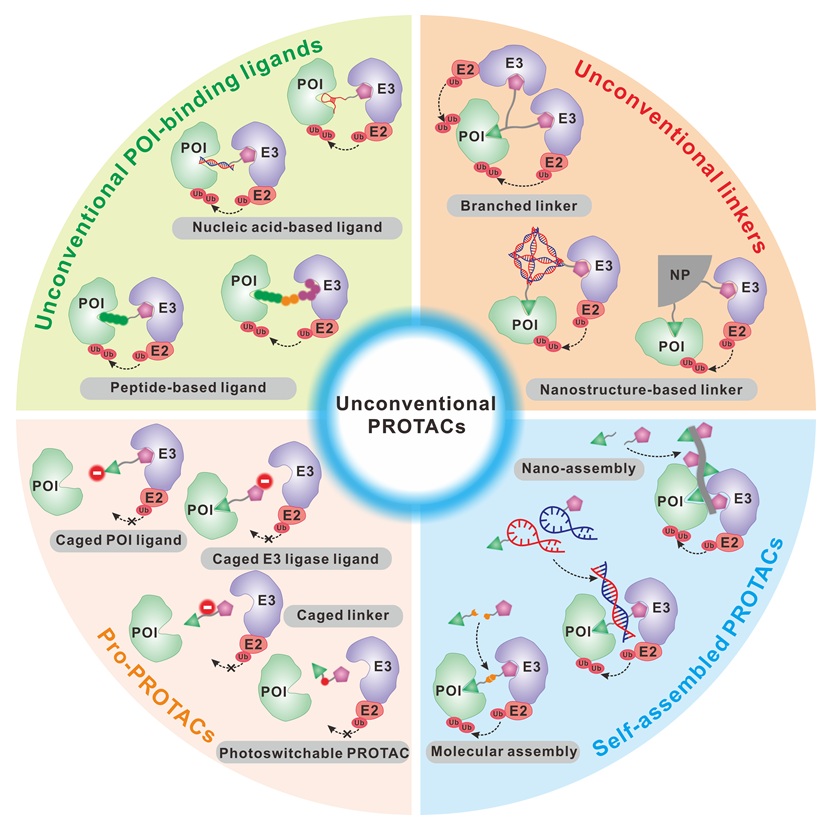
圖1. 非常規(guī)PROTAC設(shè)計�。圖片來源:Angew. Chem. Int. Ed.
本文要點
1)具有非常規(guī)結(jié)合配體的 PROTACs:利用多肽或核酸替代傳統(tǒng)小分子配體開發(fā)的PROTACs受到了廣泛關(guān)注,特別是在增強(qiáng)靶點特異性和擴(kuò)大可藥物化蛋白的范圍方面�。
2)具有非常規(guī)連接體的 PROTACs:基于支鏈連接體和納米結(jié)構(gòu)連接體,有助于實現(xiàn)更好的靶點結(jié)合�����,增強(qiáng)降解效率,改善治療結(jié)果����,并擴(kuò)大PROTACs在不同治療領(lǐng)域的適用性。
3)pro-PROTACs: Pro-PROTAC是PROTAC分子的一種創(chuàng)新形式��,其配體的靶向功能通過籠狀基團(tuán)失活����,代表了前體藥物技術(shù)與基于PROTAC的策略的先進(jìn)整合����,具有選擇性和特異性提高、穩(wěn)定性和藥代動力學(xué)增強(qiáng)����、副作用減少的優(yōu)點,提高了靶向蛋白降解的安全性和有效性�����。
4)自組裝的 PROTACs:將無蛋白降解功能的前體自組裝形成具有功能的PROTAC分子或納米PROTAC結(jié)構(gòu)�,可以提高穩(wěn)定性和改善藥代動力學(xué)����,減少對合成方法的需求和潛在降解毒性���。
總結(jié)與展望
非常規(guī)PROTACs通過優(yōu)化結(jié)構(gòu)設(shè)計��,有助于克服常規(guī)PROTACs開發(fā)耗時��、生物利用度低����、藥代動力學(xué)不理想�����、鉤效應(yīng)等局限性��,提高了PROTACs在腫瘤治療中的選擇性和療效��。因此�,對非常規(guī)的PROTACs的探索在藥物發(fā)現(xiàn)和治療發(fā)展領(lǐng)域具有巨大的前景。后續(xù)可以在高效非常規(guī)配體和非常規(guī)連接體的擴(kuò)展�、共價預(yù)偶聯(lián)策略、不依賴內(nèi)源性E3連接酶的PROTACs開發(fā)、輔助給藥和輔助治療系統(tǒng)的發(fā)展以及體內(nèi)應(yīng)用和臨床試驗方面��,進(jìn)行更加深入的研究����,以充分實現(xiàn)PROTAC在臨床中的潛力。隨著分子設(shè)計變得更加精準(zhǔn)���,PROTACs有望改變許多目前難治性疾病的治療格局���。
這一綜述近期發(fā)表在Angew. Chem. Int. Ed.上,文章的第一作者是天津大學(xué)博士后張旭����,通訊作者是天津大學(xué)王生教授���、新加坡國立大學(xué)陳小元院士�、清華大學(xué)喻國燦教授���、新加坡國立大學(xué)鄒建華博士�。
Unconventional PROTACs for Targeted Protein Degradation in Cancer Therapy
Xu Zhang, Zhangzhi Song, Xinyu Zhang, Jianhua Zou, Guocan Yu, Xiaoyuan Chen, and Sheng Wang
Angew. Chem. Int. Ed. 2025, DOI: /10.1002/anie.202507702
以上內(nèi)容轉(zhuǎn)載自https://www.x-mol.com/news/923492
版權(quán)歸原作者所有�����,如有任何問題,請聯(lián)系我們����!
優(yōu)南推薦產(chǎn)品