磺酰胺類分子的研究背景
當前癌癥治療主要面臨著耐藥性和藥物脫靶毒性兩大主要挑戰(zhàn)�����,而磺酰胺類化合物結構多樣�、藥效廣泛�,有望成為更高效低毒的抗癌分子����。磺酰胺類分子作為靶向藥物和農(nóng)藥的主要活性成分�����,常被用作羧酸基團的有效生物等排體����,能夠避免羧酸基團的代謝不穩(wěn)定性�����、跨膜擴散受限和毒性等問題���。目前部分化合物已被開發(fā)為HDAC抑制劑以及拓撲異構酶 II抑制劑等上市藥物����,在抗菌���、抗癲癇以及抗腫瘤等領域中被廣泛應用���。
磺酰胺類衍生物一:芳香化酶抑制劑
乳腺癌作為全球女性中較為嚴重的惡性腫瘤之一,與體內(nèi)雌激素濃度過高密切相關���。而芳香化酶(Aromatase, 又稱 CYP19)負責將雄激素催化轉(zhuǎn)化為雌激素�,在雌激素生物合成中發(fā)揮核心作用,因此�����,通過抑制芳香化酶來降低雌激素水平已成為治療乳腺癌的有效策略���。然而����,盡管芳香化酶抑制劑展現(xiàn)出良好的臨床療效�����,但在長期使用過程中仍面臨獲得性耐藥和一些副作用���,近年來�����,基于磺酰胺基團優(yōu)良的藥物構效特性���,研究者開發(fā)了多種基于磺酰胺的芳香化酶抑制劑�。
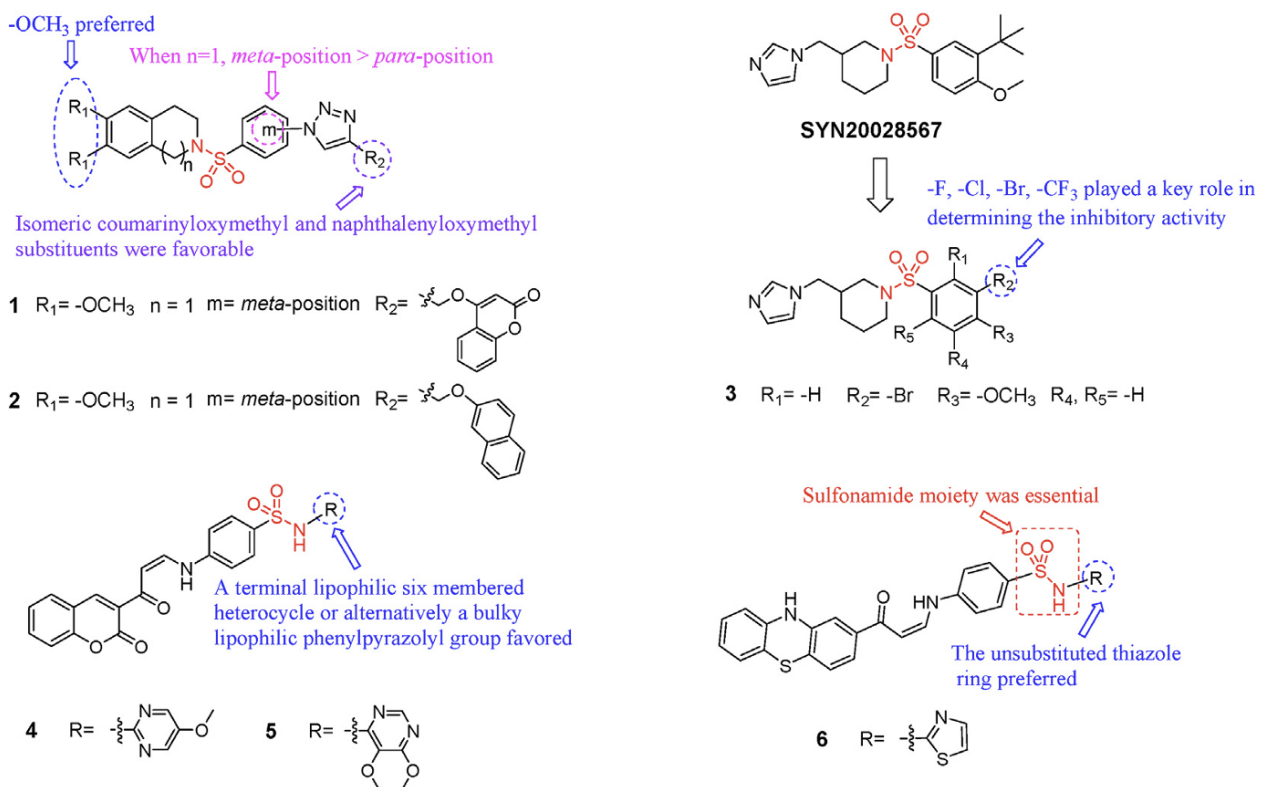
圖1 部分基于磺酰胺的芳香化酶抑制劑
Di Matteo 等人通過以已知的先導化合物SYN20028567為基礎��,設計并合成了一系列基于咪唑基哌啶結構的磺酰胺衍生物���,通過半自動化高通量篩選(HTS)進行抑制活性評估,發(fā)現(xiàn)化合物3最具活性�。
此外,在 Pingaew 等人發(fā)現(xiàn)的構效關系基礎上�,Ghorab 等人又開發(fā)出一類含有色原烯(chromene)骨架的磺酰胺衍生物作為芳香化酶抑制劑,通過T47D 乳腺癌細胞系評估其抗增殖活性�,發(fā)現(xiàn)這類化合物均表現(xiàn)出良好的芳香化酶抑制活性,其中化合物 4 和 5 表現(xiàn)最優(yōu)��。進一步的SAR 分析表明���,在末端引入疏水性六元雜環(huán)或體積較大的苯基吡唑基團����,有助于提高芳香化酶抑制活性和乳腺癌細胞的抗增殖作用��。
磺酰胺類衍生物二:碳酸酐酶抑制
腫瘤微環(huán)境中的低氧特征在癌癥的發(fā)生和發(fā)展中起著關鍵作用���,癌細胞能通過降低胞內(nèi)pH值并改變基因表達方式以適應對正常細胞不利的環(huán)境�����。其中����,碳酸酐酶(CA)作為一類鋅金屬酶,能夠通過催化二氧化碳與水的可逆轉(zhuǎn)化反應來調(diào)節(jié)細胞內(nèi)外的pH值���。其中���,CA IX和CA XII在多種腫瘤中表達上調(diào),能促進腫瘤的生長��、增殖�����、侵襲�、轉(zhuǎn)移,并使腫瘤細胞獲得對放化療的耐受性���,因此被認為是重要的抗癌靶點���,近年來已有大量以磺酰胺類結構為核心的抑制劑被開發(fā)出來�����。
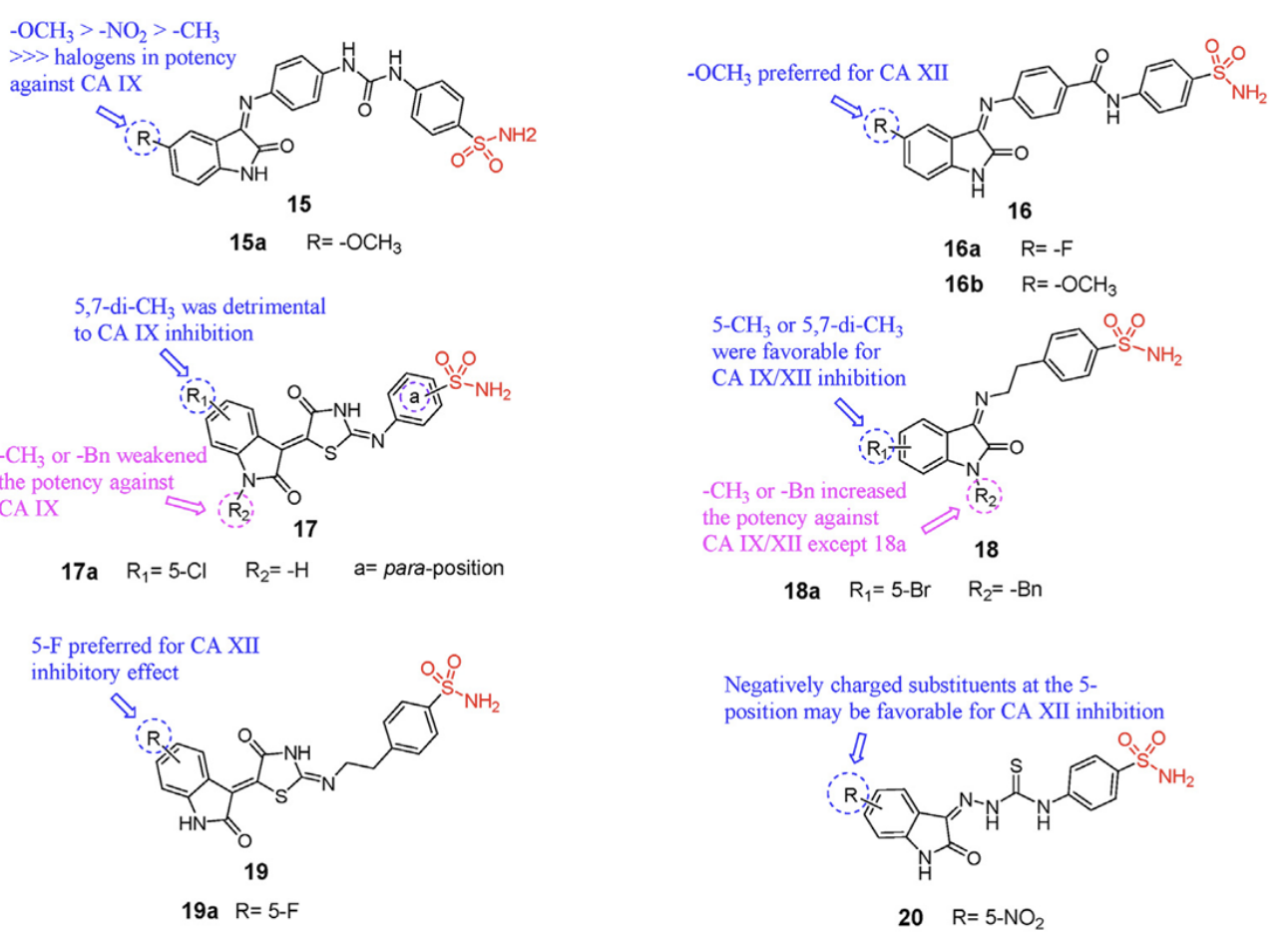
圖2 基于磺酰胺的碳酸酐酶抑制劑
Eldehna等人采用分子雜交策略設計合成了兩類帶有異吲哚酮基團的苯磺酰胺衍生物(圖2化合物15和16)�����,經(jīng)過抑制活性測試,15a和16a分別是兩個系列中對CA IX抑制效果最強的化合物�����。隨后�,該團隊進一步合成了一系列含有異吲哚酮-噻唑烷酮結構的磺酰胺類化合物(圖2化合物17),其對CA II和CA IX表現(xiàn)出更優(yōu)的抑制效果��。
雜芳基磺酰胺類的合成路徑與優(yōu)化
傳統(tǒng)藥物合成方法通常依賴雜芳基磺酰氯與胺制備磺酰胺(圖 3A)�,但這種試劑并不穩(wěn)定且具有毒性,不適合大規(guī)模的工業(yè)化操作����。隨后,一鍋法合成策略(圖 3B)以及基于銅催化的芳基硼酸和DABSO(硫代二亞磺酸鹽)的方法被陸續(xù)提出�,更有后來電化學氧化偶聯(lián)法的發(fā)展(圖 3C)��,這些方法為磺酰胺的合成提供了無毒替代路線�����。然而�����,盡管磺酰胺的合成技術已有顯著進步����,多雜原子雜芳基磺酰胺的合成仍是難題����,需要更高效、溫和且安全的策略��。

圖3 以往的磺酰胺類藥物合成路線
N,N-二取代芳雜基磺酰胺合成新方法
氧化偶聯(lián)合成法利用雜芳基硫醇和伯胺得到N-單取代磺酰胺�,解決了 N-取代雜芳基磺酰胺的“初步構建難題”。然而進一步的取代卻仍待探索�����。近年來�,捷克科學院���、帕拉茨基大學的Roman O. Iakovenko團隊提出了微波促進的Fukuyama–Mitsunobu烷基化法,用于進一步合成N,N-二取代的苯并噻唑-2-基磺酰胺����,尤其是結構不穩(wěn)定的苯并惡唑磺酰胺,且產(chǎn)物且兼容立體選擇性�����,保留光學純度��。該方法首先用烷基封住N-單取代磺酰胺上酸性較高的N-H�����,避免其結構受到周圍環(huán)境影響而降解�����。
反應條件稍作修改后�����,成功轉(zhuǎn)化為 (+)-17f�����,產(chǎn)率 48%��,產(chǎn)物穩(wěn)定 3個月����。合成過程中用到的起始原料苯并噻唑-2-硫醇和烷基胺(alkyl amines),均為易得的大宗化學品��,流程簡單高效����,條件溫和,能夠高效構建多種類型的雜芳基磺酰胺結構單元�����,預期將進一步推動其在藥物化學等相關領域的開發(fā)與應用�����。
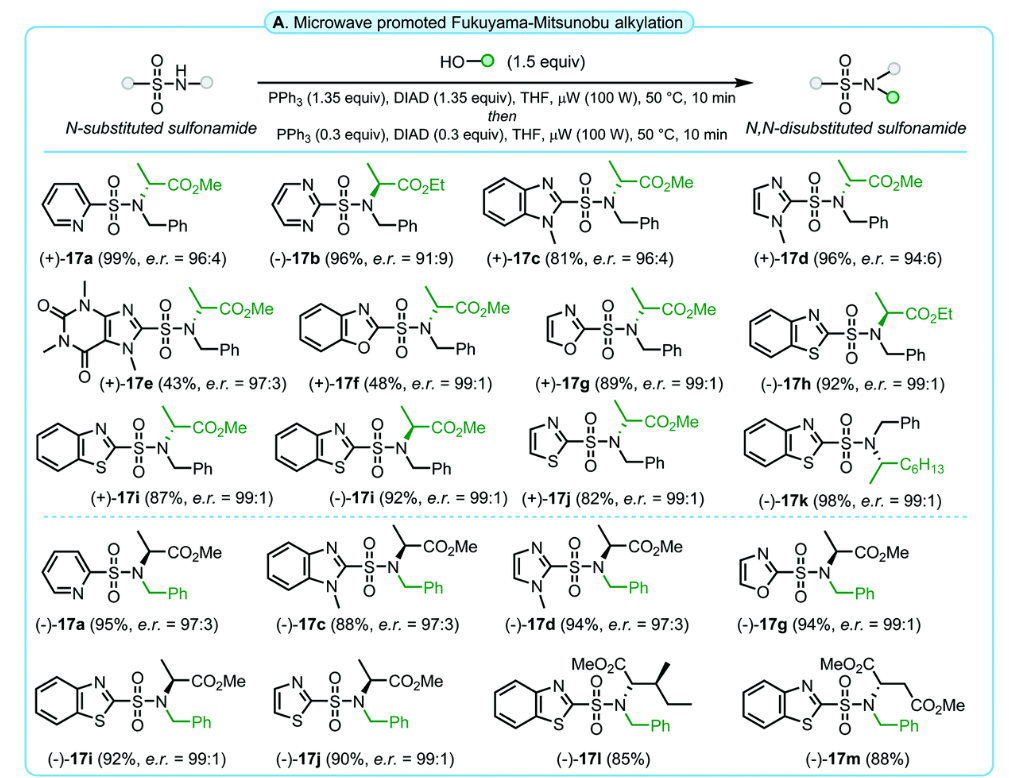
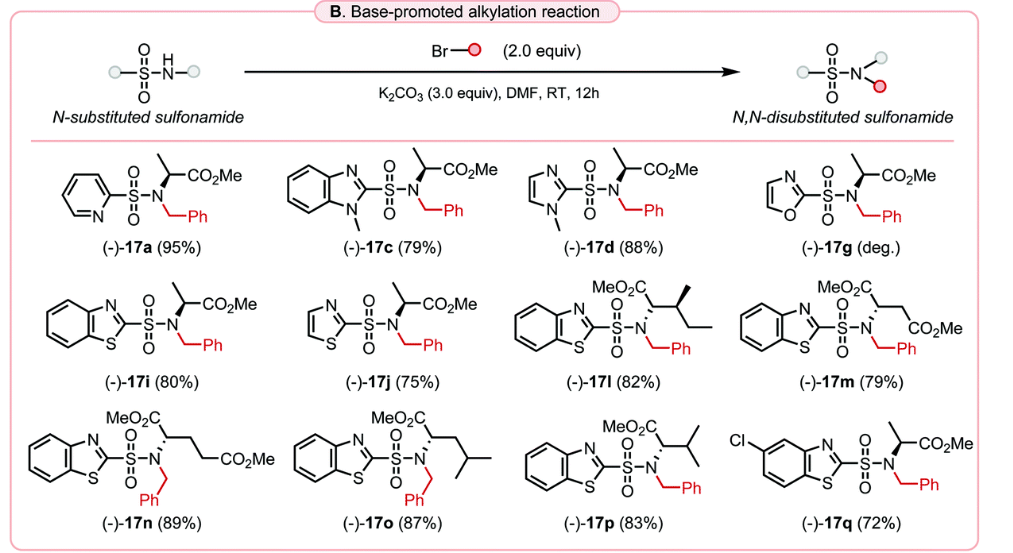
圖4 N,N-二取代磺酰胺的合成
相關產(chǎn)品推薦
參考文獻
1. 10.1021/acs.jnatprod.7b00921IF: 3.6 Q1
2. 10.1002/cmdc.201200585IF: 3.4 Q2
3. 10.1016/j.ejmech.2015.08.010IF: 5.9 Q1
4. 10.1016/j.jinorgbio.2009.10.011IF: 3.2 Q2
5. 10.1016/j.ejmech.2016.10.020IF: 5.9 Q1
6. 10.1007/s00109-007-0281-3IF: 4.2 Q1
7. 10.1039/d2ob00345gIF: 2.7 Q2