研究背景
親核氮中心功能化是藥物化學(xué)等領(lǐng)域調(diào)控分子結(jié)構(gòu)功能的主要策略����,其在藥物后期功能化等方面愈發(fā)重要�����。但胺的烷基化反應(yīng)存在副反應(yīng)多�、條件苛刻等問題,尤其制備α-手性胺時(shí)挑戰(zhàn)更大�。雖已有通過手性銅催化體系證明自由基催化方法在胺的不對(duì)稱N-烷基化中的潛力,且脫羧N-烷基化也成為有效方法����,但不對(duì)稱脫羧C(sp³)-N官能化仍難實(shí)現(xiàn)。沈陽藥科大學(xué)金盛飛/程卯生/美國(guó)UTSA Oleg V. Larionov團(tuán)隊(duì)報(bào)道了一種由鈷(salen)/吖啶光催化體系促進(jìn)的不對(duì)稱脫羧N-烷基化反應(yīng),首次實(shí)現(xiàn)弱親核芳香胺與外消旋羧酸的直接對(duì)映匯聚N-烷基化�����,為合成α-手性芐胺提供新途徑�。(圖1)。

圖1 胺的氮-烷基化策略
條件篩選
以乙腈為溶劑�,吖啶A1和含二苯并呋喃的配合物Co1為催化劑時(shí),羧酸1與苯胺2反應(yīng)生成N-烷基化產(chǎn)物3a�����,產(chǎn)率98%���,ee值90%���。對(duì)照實(shí)驗(yàn)證實(shí),光�����、吖啶�����、鈷和氧化劑是產(chǎn)物形成的關(guān)鍵因素��,其他吖啶催化劑效率較低���。亞化學(xué)計(jì)量的外消旋樟腦磺酸(CSA)可抵消胺對(duì)吖啶催化脫羧的抑制作用以實(shí)現(xiàn)高產(chǎn)率�����,且其對(duì)映體純度不影響反應(yīng)的對(duì)映選擇性���。二氯甲烷和乙酸乙酯等溶劑會(huì)降低產(chǎn)率和對(duì)映選擇性,反應(yīng)溫度也會(huì)影響產(chǎn)率和對(duì)映選擇性��。催化劑結(jié)構(gòu)對(duì)高對(duì)映選擇性至關(guān)重要�����,苯環(huán)鄰位帶二苯并呋喃取代基的1,2-二苯乙二胺基催化劑表現(xiàn)優(yōu)異�。例如,反式-1,2-環(huán)己二胺衍生的催化劑Co2得到幾乎外消旋的產(chǎn)物(9% ee)�����,催化劑Co3和Co4的ee值為26%和62%���。salen配體結(jié)構(gòu)影響催化性能��,替換遠(yuǎn)端叔丁基或調(diào)整取代基會(huì)改變立體選擇性�,使用5和5'位置未取代的salen配體的催化劑Co9性能最佳(圖2)。
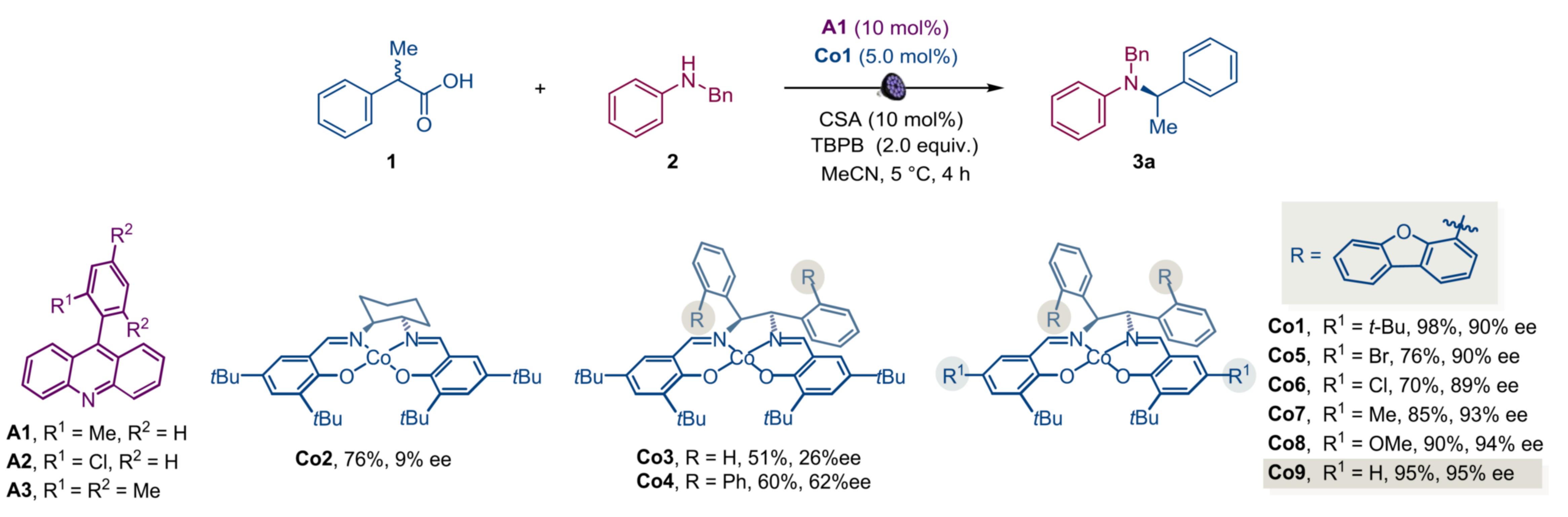
圖2 條件篩選
底物范圍

圖3 底物拓展-舉例
在確定最佳條件后���,作者探索了對(duì)映匯聚脫羧N-烷基化反應(yīng)的范圍�����。多種 N-烷基苯胺��,如位阻大的異丙基衍生物���、帶各類取代基(鹵素、烷氧基等)的苯胺���、多取代苯胺�����、含酯基等基團(tuán)的苯胺及二芳基胺等����,均能以良好至優(yōu)異產(chǎn)率和對(duì)映選擇性得到手性胺���,而脂肪胺產(chǎn)率和對(duì)映選擇性較低��。烷基自由基前體方面�����,帶各類對(duì)位����、間位�����、鄰位取代基的羧酸�����,氟比洛芬類似物�、多環(huán)芳烴酸、二取代芳基底物及α碳帶其他烷基的自由基前體均適用��。該方法還適用于多種生物活性骨架�,如非甾體抗炎藥��、抗癌藥����、退熱劑等衍生物�,展現(xiàn)出廣泛適用性(圖3)。
機(jī)理實(shí)驗(yàn)

圖4 機(jī)理實(shí)驗(yàn)
作者隨后開展機(jī)理研究(圖4)�,TEMPO加入抑制脫羧N-烷基化并生成烷基自由基-TEMPO加合物。 EPR光譜分析使用N-叔丁基-α-苯基硝酮作自旋捕獲劑���,證實(shí)烷基自由基和叔丁氧基自由基參與反應(yīng)�。不同對(duì)映體純度鈷催化劑實(shí)驗(yàn)顯示��,產(chǎn)物3a的ee值與催化劑ee值呈線性關(guān)系�,表明催化過程涉及單個(gè)鈷催化劑分子且無顯著催化劑聚集。對(duì)1,4-碳胺化反應(yīng)的機(jī)理研究確立了烷基鈷(IV)介導(dǎo)芳香胺N-烷基化的可行性��。Hammett圖負(fù)斜率表明酸衍生烷基起親電作用����。通過實(shí)驗(yàn)排除烷基鈷(III)中間體途徑,證明烷基鈷(IV)中間體由鈷(III)催化劑直接捕獲自由基形成����。
密度泛函理論計(jì)算

圖5 DFT計(jì)算
計(jì)算研究旨在探究鈷催化自由基-極性交叉過程的立體誘導(dǎo)機(jī)制(圖5)�。先前研究表明��,鈷(IV)中間體可通過自由基加成鈷(III)催化劑(由Co(II)經(jīng)單電子轉(zhuǎn)移生成)形成���。芐基自由基10與鈷(III)反應(yīng)生成非對(duì)映體中間體Co-R和Co-S,后者動(dòng)力學(xué)更占優(yōu)�,隨后烷基轉(zhuǎn)移至苯胺生成產(chǎn)物,催化劑經(jīng)單電子轉(zhuǎn)移周轉(zhuǎn)���。畸變-相互作用活化應(yīng)變模型(ASM)分析顯示�,過渡態(tài)TSA因催化劑片段與芐基自由基間更強(qiáng)相互作用及更小畸變��,活化能低于TSB�。能量分解分析(EDA) 表明TSA的電荷轉(zhuǎn)移和色散作用抵消靜電排斥,且泡利排斥更弱��。非共價(jià)相互作用(NCI)分析發(fā)現(xiàn)���,二苯并呋喃通過π-π作用穩(wěn)定催化劑��,TSA與鄰位二苯并呋喃的相互作用更強(qiáng)��,減少排斥����。
總結(jié)
本研究開發(fā)了芳香胺的對(duì)映匯聚脫羧N-烷基化反應(yīng),通過吖啶光催化與鈷催化的自由基-極性交叉(RPC)結(jié)合�����,無需預(yù)活化胺或羧酸�����,在溫和條件下高效合成多種具有藥物及合成價(jià)值的α-手性芐胺�����。機(jī)理研究揭示�����,手性Co (salen)催化劑中1,2-二芳基乙二胺單元的結(jié)構(gòu)與電子效應(yīng)通過色散作用和泡利排斥效應(yīng)協(xié)同調(diào)控對(duì)映選擇性�,其鄰聯(lián)芳基片段與烷基自由基間的吸引相互作用是立體控制的關(guān)鍵。計(jì)算研究進(jìn)一步證實(shí)����,配體內(nèi)聯(lián)芳基的π-π相互作用及自由基與配體的色散作用促進(jìn)了高對(duì)映選擇性轉(zhuǎn)化。
文獻(xiàn)詳情
作者:Siwen Huang, Ramon Trevino, Dishun Zuo, Xin Tian, Wenhan Yang, William B. Hughes, Seth O. Fremin, Arka Porey, Vy T. B. Nguyen, Bo Gao, Xiyuan Xu, Babu Raj Dhungana, Yingqian Jiang, Yao Sun, Chao Huang, Min He, Chandan Giri, Shree Krishna Dhakal, Bin Qin, Yongxiang Liu, Maosheng Cheng,* Oleg V. Larionov,* and Shengfei Jin*
題目:Cobalt-Catalyzed Enantioconvergent Decarboxylative N?Alkylation
DOI:10.1021/jacs.5c06317 (https://doi.org/10.1021/jacs.5c06317)